Iguazú (LaVozDeCataratas) Luego del escándalo desatado por el “Vacunatorio VIP” que funcionó en el Hospital Posadas de Haedo y en el Ministerio de Salud, que le costó el despido al ministro Ginés González García, la nueva ministra Carla Vizzotti aprobó la vacuna china el domingo pasado tras las sugerencias de la ANMAT. Ahora, parte de la estrategia gubernamental pasa por intensificar el control de la aplicación de las dosis disponibles y que se transparente el accionar. Por eso esta semana también se espera la llegada de otras 300 mil dosis de la vacuna rusa, Sputnik V.
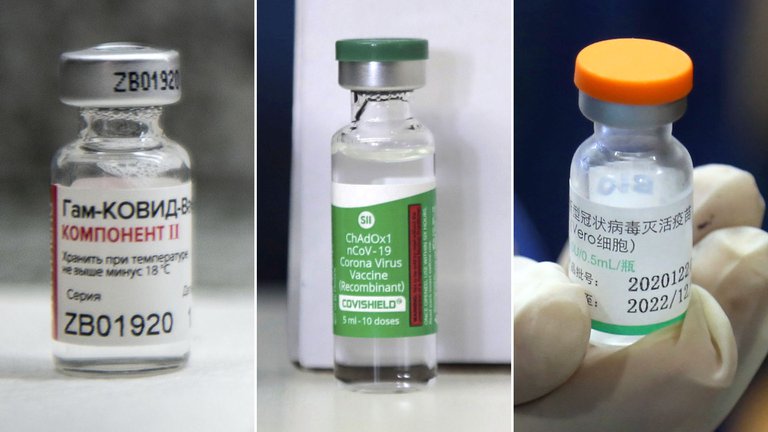
¿Pero, de qué se trata la vacuna china de Sinopharm y qué diferencias tiene con la Sputnik V, que ya se aplica, y la que ya llegó al país la semana última proveniente de India, Covishield?
Sinopharm: La vacuna China
La vacuna SARS COV-2 desarrollada por Sinopharm en colaboración con el Laboratorio Beijing Institute of Biological Products de China es una vacuna “inactivada”, lo que significa que porta una versión del virus alterada genéticamente que le impide reproducirse y desarrollar la enfermedad, pero que genera una “respuesta inmune en el organismo con capacidad protectora”.
Contiene una versión muerta del germen que no produce enfermedad pero genera anticuerpos y que ya se utiliza en varias vacunas como las de la gripe, hepatitis A, polio y la rabia. Es la primera vacuna en utilizar un inmunógeno proteico. Esencialmente, es una vacuna COVID-19 inactivada con virus completo, un enfoque diferente de lo que están haciendo otros candidatos avanzados.
La presidenta de la Sociedad Argentina de Vacunología y Epidemiología (SAVE), Florencia Cahn (M.N. 114.399), sostuvo: “Utilizan un virus que está previamente inactivado de modo que el virus no provoca la enfermedad pero sí genera una respuesta inmune. Los resultados interinos de Fase 3 muestran una eficacia superior al 80%. De todas maneras son datos que se siguen analizando. Pero son muy buenos resultados”.
Esta vacuna tuvo un costo de 20 dólares por dosis para nuestro país. La vacuna requiere de dos dosis que se han de aplicar con al menos 21 días de diferencia, y puede transportarse y almacenarse a entre 2 ºC y 8 °C y permanecer estable durante 24 meses.
Sputnik V: La vacuna Rusa
Sputnik V no posee ningún elemento del coronavirus en su composición, se presenta en forma liofilizada, es decir, como un polvo que se mezcla con un excipiente para disolverlo y luego administrarlo por vía intramuscular.
El fármaco utiliza una tecnología de adenovirus humano de dos vectores diferentes, Ad5 y Ad26, para una primera y una segunda inyección. Sin embargo, Sputnik V no contiene adenovirus humanos vivos, sino vectores adenovirales humanos que no son capaces de multiplicarse y son completamente seguros para la salud.
Los “vectores” son vehículos que pueden introducir material genético de otro virus en una célula. El gen del adenovirus, que es el causante de la infección, se sustrae y en su lugar se inserta un gen con el código de la proteína de otro virus. El elemento insertado es seguro para el organismo y ayuda al sistema inmunológico a reaccionar y producir anticuerpos que nos protegen de la infección.
La efectividad de la vacuna Sputnik V fue del 91,4%, dato que se confirmó en cada uno de los tres puntos de control de los ensayos clínicos. Asimismo, la eficacia de la vacuna Sputnik V contra casos graves de infección por coronavirus fue del 100%.
El problema radica en la logística que se precisa para su distribución, ya que debe estar almacenada a -18° grados y una vez abierta tiene que ser aplicada en la siguiente media hora.
Covishield: La vacuna hindú
El 9 de febrero último, el Ministerio de Salud de la Nación habilitó el uso de emergencia de la vacuna Covishield fabricada en India, mientras que el Gobierno celebró un convenio con el Serum Institute de India, el organismo encargado de producirla en colaboración con la Universidad de Oxford y AstraZeneca, “en el contexto de una transferencia tecnológica”. “Esta vacuna actualmente se presenta como una herramienta terapéutica segura y eficaz de acceso para que nuestro país baje la mortalidad, reduzca la morbilidad y disminuya la transmisibilidad de la enfermedad COVID-19 producida por el virus SARS-Cov-2″, justificó la cartera nacional sanitaria en la Resolución 627/2021, publicada en el Boletín Oficial.
La vacuna denominada “COVISHIELD/ ChAdOx1nCoV-19 Corona Virus Vaccine – Recombinant” la producen Oxford-AstraZeneca en el Serum Institute of India, el mayor fabricante de vacunas del mundo, que produce a razón de más de 50 millones de dosis al mes.
Está compuesta de una versión debilitada de un virus del resfriado común (conocido como adenovirus) de chimpancés y se ha modificado para que se parezca más al coronavirus, sin causar enfermedades. Como toda vacuna, cuando se la inyecta en el organismo, hace que el sistema inmunológico comience a producir anticuerpos y lo prepara para atacar cualquier infección por coronavirus. La misma se administra en dos dosis con entre cuatro y 12 semanas de diferencia.
Según su fabricante, se puede almacenar de manera segura a temperaturas de entre 2 °C y 8 °C, aproximadamente lo mismo que una heladera doméstica, y se puede administrar en entornos de atención médica existentes, como los consultorios médicos o farmacias, por lo que constituye una gran ventaja frente a competidores como la de Pfizer-BioNTech, que actualmente se administra en varios países, y debe almacenarse a -70 °C, moviéndose un número limitado de veces.
Los ensayos clínicos internacionales de la vacuna Oxford-AstraZeneca demostraron que cuando las personas recibieron media dosis y luego una dosis completa, la efectividad alcanzó el 90%. Pero no había suficientes datos claros para aprobar la idea de media dosis y dosis completa. Los fabricantes indios de la vacuna aseguran que Covishield es “altamente eficaz” y está respaldada por los ensayos de fase III realizados en Brasil y Reino Unido.
La vacuna producida en India y autorizada ya por 12 autoridades sanitarias en el mundo fue aprobada por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), que contó “con toda la información según lo establecido por el procedimiento para la autorización de emergencia, en relación con el cumplimiento de los estándares requeridos de las plantas elaboradoras, el desarrollo y la elaboración de los productos, su certificación en el país de origen y el cumplimiento de los estándares de calidad”, según comunicaron las fuentes oficiales. Así, la Dirección Nacional de Control de Enfermedades Transmisibles ha elaborado un informe técnico en el que consideró “recomendable proseguir con la solicitud de autorización de emergencia de la misma”.
Además, “no se han presentado eventos adversos graves, ni se han identificado diferencias significativas en la eficacia observada en los diferentes grupos etarios que participaron de los ensayos clínicos”, subraya la resolución firmada por el entonces ministro Ginés González García. El Gobierno también celebró un convenio con el Serum Institute de India, para la transferencia tecnológica de la misma.
Con Información de Infobae